 El galio es otro elemento químico en la tabla periódica, su símbolo es Ga y su número atómico es 31. Fue descubierto en Francia, en el año 1875, gracias a la espectroscopia, debido a su espectro característico al observar una blenda de zinc oriunda de los Pirineos.
El galio es otro elemento químico en la tabla periódica, su símbolo es Ga y su número atómico es 31. Fue descubierto en Francia, en el año 1875, gracias a la espectroscopia, debido a su espectro característico al observar una blenda de zinc oriunda de los Pirineos.
En ese mismo año el elemento fue aislado gracias a la electrólisis del hidróxido con una solución de hidróxido potásico.
Antes de ser descubierto, casi todas las propiedades de este elemento fueron descritas y predichas por el científico Mendeleyev. Éste lo solía llamar eka-aluminio basando sus argumentos en la posición que este elemento debía ocupar en la tabla periódica.
Indice
Configuración Electrónica del Galio
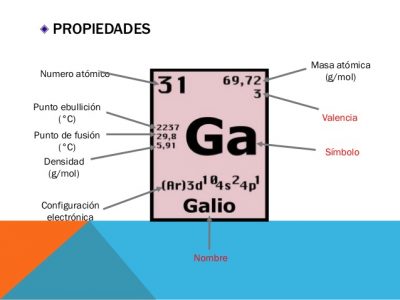 El galio es el elemento número 31 en la tabla periódica, por lo tanto su número atómico es 31. Su configuración electrónica completa es 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p1 y su configuración electrónica simplificada o abreviada es Ar 3d10 4s2 4p1.
El galio es el elemento número 31 en la tabla periódica, por lo tanto su número atómico es 31. Su configuración electrónica completa es 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p1 y su configuración electrónica simplificada o abreviada es Ar 3d10 4s2 4p1.
La configuración electrónica de los elementos de la tabla periódica define la manera en la cual los electrones se estructuran en los átomos que tienen un elemento.
El radio de Bohr o radio atómico del galio es 136 pm, el radio medio del elemento es 130 pm, su radio de Van der Waals es de 187 ppm mientras que su radio covalente es igual a 126 pm.
El galio posee total 31 electrones y su distribución se hace de la siguiente manera: la primera capa tiene 2, en la segunda hay 8, en la tercera existen 18 y en la cuarta hay 3 electrones.
Características Generales del Galio
- El galio es un metal blando. En estado líquido es grisáceo y en estado sólido es brillante y plateado.
- Es un sólido desplegable en temperaturas bajas y se funde a temperaturas que se acercan a la del ambiente del mercurio, cesio y rubidio y hasta cuando se sostiene en mano por debajo de su punto de fusión el cual es 29,7646 grados centígrados.
- El metal tiene una expansión de 3,1% cuando se solidifica y puede flotar en el líquido, igual como lo hace el hielo en el agua.
- La presión del vapor de galio es baja en altas temperaturas.
- El galio corroe demás metales cuando se difunde en las redes cristalinas.
Propiedades Químicas del Galio
- El grupo del galio es el 13, se ubica en el período 4 de la tabla periódica.
- La masa atómica del galio es 69,723 u.
- El galio forma parte de los elementos metálicos llamados metales del bloque p que se ubican junto a los semimetales o metaloides de la tabla periódica. Esta clase de elementos normalmente son blandos, tienen bajos puntos de fusión. Estas propiedades se le atribuyen al galio de igual forma.
- El estado en el que el galio se encuentra en forma natural es el sólido.
- El aspecto químico del galio es plateado y blanco.
- El número atómico del galio 31 y su símbolo químico es Ga.
- El punto de fusión de este elemento es de 29,7646 grados centígrados o de 302,9146 grados Kelvin.
- El punto de ebullición de este elemento es de 2204,85 grados Celsius o de 2477 grados Kelvin.
Obtención, Abundancia y Precauciones
Las trazas del galio son encontradas en minerales tales como el carbón, la bauxita, la esfalerita, la germanita y el diasporo. Este metal es un subproducto en los procedimientos de obtención de diversos metales. A causa de la expansión cuando se solidifica el líquido, éste no debe guardarse en recipientes que sean de vidrio o de metal ni tampoco llenar el recipiente por completo con el galio líquido debido a que puede ocasionar que éste se rompa por la expansión que este metal presenta.

